Chemia organiczna/Kwasy karboksylowe i nitryle/Nitryle - budowa, nazewnictwo i właściwości fizyczne
| Nitryle - organiczne związki chemiczne, pochodne cyjanowodoru o wzorze ogólnym R-C≡N. |

Nitryle (cyjanki) są związkami blisko spokrewnionymi z kwasami karboksylowymi, ulegają podobnym reakcjom.
Budowa nitryli
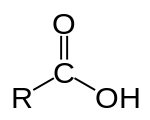
[edytuj]W skład cząsteczek nitryli wchodzi grupa cyjanowa, w której atomy węgla i azotu są połączone wiązaniem potrójnym. Atom węgla w grupie cyjanowej ma hybrydyzację sp, wobec czego kąt między wiązaniami C-C≡N wynosi 180°. Nitryle, tak jak kwasy karboksylowe, zawierają atom węgla połączony trzema wiązaniami z atomem elektroujemnym. Obie grupy, karboksylowa i cyjanowa, zawierają wiązanie π.
| Kwas karboksylowy (trzy wiązania do dwóch atomów tlenu) |
Nitryl (trzy wiązania do jednego atomu azotu) |
|---|---|
 |
Nazewnictwo nitryli
[edytuj]Nitryle można nazywać na różne sposoby. Pierwszy z nich, zalecany przez IUPAC, polega na dodaniu przyrostka -nitryl do nazwy macierzystego węglowodoru. Atom węgla w grupie cyjanowej jest oznaczany numerem 1.
 |
 |
 |
| Acetonitryl | Butanonitryl | Benzonitryl |
W bardziej złożonych przypadkach nazwy nitryli tworzy się od nazwy analogicznego kwasu karboksylowego. Wówczas nazwę kwas ...karboksylowy zastępuje się nazwą -karbonitryl. Atom węgla grupy cyjanowej nie wchodzi w skład głównego łańcucha węglowego, zaś sama grupa jest traktowana jak podstawnik przy atomie węgla C1. Przykładem jest poniższy związek, 2,2-dimetylocykloheksanokarbonitryl, który pochodzi od kwasu 2,2-dimetylocykloheksanokarboksylowego.
Drugi sposób polega na nazywaniu nitryli jak pochodnych alkanów. Grupa cyjanowa jest traktowana jak podstawnik łańcucha węglowego, a atom węgla tej grupy nie jest częścią głównego łańcucha. W tym przypadku nazwa przyjmuje postać "cyjanek alkilu". Jest to system nazewnictwa podobny do stosowanego wobec halogenków alkilowych.
 |
 |
 |
| Cyjanek metylu | Cyjanek propylu | Cyjanek fenylu |
Gdy grupa -C≡N nie jest uznawana jako grupa główna, to jest ona traktowana jako podstawnik, a do nazwy dodaje się przedrostek cyjano-. Przykładem może być 1,2-dicyjanobenzen, w którym grupy cyjanowe potraktowano jako podstawniki pierścienia aromatycznego benzenu.

Dalszym przykładem może być 3-(cyjanometylo)heksanodinitryl.
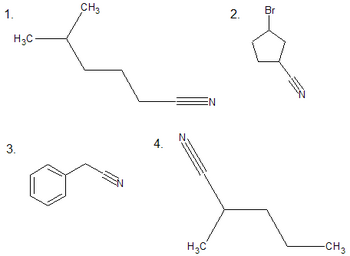
Ćwiczenie
|
Właściwości fizyczne
[edytuj]Nitryle o niższej liczbie atomów węgla są dobrze rozpuszczalnymi w wodzie cieczami o przyjemnej woni. Wyższe nitryle alifatyczne to ciała stałe. Temperatury wrzenia niższych cyjanków są dość wysokie jak na związki o małej masie cząsteczkowej, co wynika z ich wysokiej polarności.
Nitryle są substancjami toksycznymi, znacznie jednak słabszymi od cyjanowodoru.